Notícias
Notícias

wthats 55 11 9386 8744 Juquitiba SP

PEPTÍDEOS BIORREGULADORES ÓRGÃO-ESPECÍFICOS E PEPTÍDEOS REGENERATIVOS NA MEDICINA VETERINÁRIA
Revisão Sistemática Abrangente, Bases Moleculares, Evidências Experimentais e Perspectivas Translacional
PETCLUBE – CIÊNCIA, GENÉTICA E BEM-ESTAR ANIMAL
AUTORES:
Cláudio Amichetti Júnior
Médico-Veterinário Integrativo. Registro profissional: CRMV-SP 75.404 VT; MAPA 00129461/2025; CREA 060149829-SP (Engenheiro Agrônomo). Atuação Continua em Nutrição, Canabinóide e Medicina Translacional Pesquisador em peptídeos biorreguladores e terapias regenerativas veterinárias.
Dr. Gabriel Amichetti
Médico-veterinário – CRMV-SP 45.592 VT. Especialização em Ortopedia e Cirurgia de Pequenos Animais
Clínica 3RD – Vila Zelina, São Paulo, Brasil.
Autor Correspondente: dr.claudio.amichetti@gmail.com
PERIÓDICO: Petclube – Ciência, Genética e Bem-Estar Animal
São Paulo, Brasil | 2024
RESUMO
A bioregulação peptídica representa uma área emergente da biotecnologia médica e da medicina regenerativa. Pequenos peptídeos reguladores derivados de tecidos específicos têm demonstrado capacidade de modular processos celulares fundamentais, incluindo expressão gênica, homeostase metabólica, reparação tecidual e modulação imunológica. Grande parte das pesquisas nesse campo foi conduzida por cientistas russos, particularmente sob liderança do gerontologista Vladimir Khavinson, no Saint Petersburg Institute of Bioregulation and Gerontology, onde foram descritos diversos peptídeos denominados citomédicos ou biorreguladores. Esses peptídeos, frequentemente constituídos por dipeptídeos ou tripeptídeos, apresentam propriedades organotrópicas, ou seja, afinidade funcional por tecidos específicos como fígado, rins, cérebro, retina, pulmões e sistema cardiovascular. Estudos experimentais sugerem que tais moléculas podem atuar por mecanismos epigenéticos, modulando diretamente a expressão gênica e restaurando funções celulares comprometidas pelo envelhecimento ou por processos patológicos. Adicionalmente, peptídeos regenerativos modernos como BPC-157, TB-500 e GHK-Cu têm demonstrado grande potencial em ortopedia e reparação tecidual. Esta monografia apresenta uma revisão sistemática abrangente das evidências experimentais e clínicas disponíveis na literatura internacional, discutindo os principais peptídeos biorreguladores órgão-específicos e regenerativos, seus mecanismos moleculares, incluindo aprofundamento em epigenética, e seu potencial translacional para aplicações na medicina veterinária.
Palavras-chave: bioregulação peptídica, regeneração tecidual, epigenética, citomédicos, BPC-157, TB-500, GHK-Cu, medicina veterinária integrativa, ortopedia veterinária.
ABSTRACT
Peptide bioregulation represents an emerging field in medical biotechnology and regenerative medicine. Small regulatory peptides derived from specific tissues have demonstrated the ability to modulate fundamental cellular processes, including gene expression, metabolic homeostasis, tissue repair, and immune modulation. Much of the research in this field has been conducted by Russian scientists, particularly under the leadership of gerontologist Vladimir Khavinson, at the Saint Petersburg Institute of Bioregulation and Gerontology, where various peptides termed cytomedins or bioregulators were described. These peptides, often composed of dipeptides or tripeptides, exhibit organotropic properties, meaning functional affinity for specific tissues such as the liver, kidneys, brain, retina, lungs, and cardiovascular system. Experimental studies suggest that such molecules can act through epigenetic mechanisms, directly modulating gene expression and restoring cellular functions compromised by aging or pathological processes. Additionally, modern regenerative peptides like BPC-157, TB-500, and GHK-Cu have shown great potential in orthopedics and tissue repair. This monograph provides a comprehensive systematic review of experimental and clinical evidence available in international literature, discussing the main organ-specific and regenerative bioregulatory peptides, their molecular mechanisms, including an in-depth look at epigenetics, and their translational potential for applications in veterinary medicine.
Keywords: peptide bioregulation, tissue regeneration, epigenetics, cytomedins, BPC-157, TB-500, GHK-Cu, integrative veterinary medicine, veterinary orthopedics.
1 INTRODUÇÃO
A medicina veterinária contemporânea transita de um modelo meramente reativo para um modelo regenerativo e integrativo. O uso de peptídeos — cadeias curtas de aminoácidos com alta biodisponibilidade — permite a sinalização celular direta sem a complexidade imunogênica de proteínas maiores. Esta monografia estabelece a base científica para o uso dessas moléculas como ferramentas de precisão na restauração de tecidos e órgãos.
A pesquisa de peptídeos biorreguladores iniciou-se na década de 1970, no Instituto de Bioregulação e Gerontologia de São Petersburgo, sob a liderança de Vladimir Khavinson. Descobriu-se que extratos peptídicos de tecidos jovens podiam restaurar a função de órgãos em animais senis através de mecanismos epigenéticos.
2 MECANISMOS MOLECULARES E EPIGENÉTICA
O diferencial dos peptídeos biorreguladores é sua capacidade de interagir com a cromatina.
2.1 Regulação Epigenética e Transcrição Gênica
Os peptídeos biorreguladores modulam a acetilação de histonas, permitindo que genes de reparo "silenciados" pelo envelhecimento ou doença sejam reativados. O GHK-Cu, por exemplo, regula para cima genes de reparo de DNA e para baixo genes pró-inflamatórios como o NF-κB.
2.2 Proteção e Otimização da Função Mitocondrial
Na Doença Renal Crônica (DRC), peptídeos como o SS-31 (Elamipretide) focam na integridade das cristas mitocondriais, prevenindo a apoptose tubular e a progressão da fibrose renal através da estabilização da cardiolipina.
2.3 Modulação do Sistema Imunológico
Peptídeos como o Thymalin atuam na restauração da função tímica, equilibrando as respostas Th1/Th2 e reduzindo citocinas pró-inflamatórias.
3 PEPTÍDEOS BIORREGULADORES ÓRGÃO-ESPECÍFICOS (CITOMÉDICOS)
A escola russa desenvolveu uma série de peptídeos com afinidade tecidual específica:
- Livagen (Fígado): Regeneração de hepatócitos e redução de fibrose.
- Renisamin (Rins): Proteção do epitélio tubular e modulação do metabolismo nitrogenado.
- Cortexin (Cérebro): Neuroproteção e plasticidade sináptica.
- Retinalamin (Retina): Melhora da microcirculação ocular.
- Vasalamin (Vasos Sanguíneos): Estabilização do endotélio.
- Bronchogen (Pulmões): Regeneração epitelial pulmonar.
- Epitalon (Glândula Pineal): Regulação do ciclo sono-vigília.
- Thymalin (Timo): Modulação imunológica.
4 PEPTÍDEOS REGENERATIVOS EM ORTOPEDIA
4.1 BPC-157 (Body Protection Compound-157)
Derivado do suco gástrico, é extremamente estável. Atua na angiogênese (via VEGF) e acelera a cicatrização de tendões, ligamentos e fístulas. Na veterinária, é o padrão-ouro para pós-operatórios ortopédicos complexos.
4.2 TB-500 (Thymosin Beta-4)
Regulador da actina, promove a migração celular para o sítio da lesão. Aumenta a deposição de colágeno organizado e reduz a inflamação sistêmica. Amplamente utilizado em equinos para tratamento de tendinites e desmites.
4.3 GHK-Cu (Copper Peptide)
Regula a expressão de mais de 4.000 genes, promovendo síntese de colágeno, elastina e glicosaminoglicanos. Excelente para regeneração cutânea e ocular.
5 COMPARATIVO: ESCOLA RUSSA vs. ESCOLA CHINESA
A pesquisa de peptídeos não é monocrática. Existem distinções fundamentais entre as duas maiores potências científicas no setor:
5.1 Escola Russa (Khavinson): Foco na Longevidade Órgão-Específica
Baseada no Instituto de Gerontologia de São Petersburgo, foca em extratos naturais ou sintéticos curtos (di e tripeptídeos) que mimetizam a sinalização de órgãos jovens.
- Mecanismo: Interação direta com a cromatina e regulação da metilação do DNA.
- Exemplos: Renisamin (Rim), Cortexin (Cérebro), Epitalon (Pineal).
5.2 Escola Chinesa (Biotecnologia Recombinante): Foco na Regeneração Sistêmica
A China consolidou-se na produção de peptídeos recombinantes de alta massa molecular e análogos sintéticos (como o NL005, análogo da Timosina Beta-4).
- Foco: Farmacocinética, segurança em larga escala e uso de scaffolds para liberação controlada.
- Aplicações: Regeneração de tecidos moles, angiogênese e cicatrização acelerada para fins militares e esportivos.
6 COMPARATIVO: PEPTÍDEOS vs. CÉLULAS-TRONCO vs. PRP
O paradigma epigenético dos peptídeos difere fundamentalmente do efeito parácrino das MSCs. Enquanto os peptídeos atuam como chaves moleculares que reativam genes de reparo, as MSCs funcionam como "fábricas" de sinalização, secretando vesículas extracelulares com miRNAs e citocinas.
Na DRC felina, a administração intravenosa de MSCs enfrenta o "first-pass effect", onde a maioria das células fica retida nos pulmões. Isso explica por que, embora as MSCs melhorem a proteinúria, a regeneração funcional do néfron ainda é um desafio. Os peptídeos oferecem uma alternativa de terapia de manutenção contínua e acessível.
| Critério | Peptídeos (Rússia/China) | Células-Tronco (MSCs) | PRP (Plasma Rico em Plaquetas) |
|---|---|---|---|
| Ação em Ligamentos | Alta: BPC-157/TB-500 aceleram angiogênese e colágeno. | Excelente: Regeneração estrutural e redução de recidivas. | Moderada: Fatores de crescimento imediatos; ação curta. |
| Ação na DRC | Epigenética: Renisamin protege o epitélio tubular. | Imunomodulação: Reduz fibrose, mas eficácia na TFG é mista. | Baixa: Pouca evidência para uso sistêmico em DRC. |
| Tipo de Terapia | Molécula sinalizadora estável. | Células vivas (Autólogas ou Alogênicas). | Concentrado autólogo de plaquetas. |
| Logística | Fácil (Liofilizado, sem cadeia de frio). | Complexa (Cultura celular, criopreservação). | Simples (Centrifugação no local). |
| Via Intracelular | Regulação Gênica / VEGF. | Efeito Parácrino / TGF-β. | Sinalização de Receptores de Superfície. |
7 APLICAÇÕES VETERINÁRIAS E PROTOCOLOS
A aplicação de peptídeos biorreguladores e regenerativos oferece intervenções terapêuticas precisas para diferentes espécies animais, com protocolos específicos para cada condição clínica.
| Espécie | Peptídeo Principal | Indicação Clínica | Protocolo Sugerido |
|---|---|---|---|
| Cães | BPC-157 + Cortexin | Ortopedia e Disfunção Cognitiva | BPC: 10-20mcg/kg/dia (SubQ); Cortexin: 5-10mg (IM) |
| Gatos | Renisamin + Vasalamin | Doença Renal Crônica (DRCF) | Renisamin: 10mg/dia; Vasalamin: 5mg/dia (Ciclos de 10 dias) |
| Equinos | TB-500 + BPC-157 | Lesões Tendíneas e Ligamentares | TB-500: 4-8mg/semana (Loading); BPC: 2-5mg/dia |
| Aves | Bronchogen | Afecções Respiratórias Crônicas | Nebulização ou via oral (dosagem ajustada por peso) |
| Bovinos | Livagen | Recuperação Metabólica Pós-Parto | Administração parenteral para suporte hepático |
8 SEGURANÇA E TOXICIDADE
Estudos de toxicidade aguda e crônica demonstram que os peptídeos biorreguladores possuem um índice terapêutico altíssimo. Por serem fragmentos de aminoácidos naturais, não sobrecarregam as vias de desintoxicação hepática ou renal.
- Efeitos Colaterais: Raramente relatados, limitando-se a irritação leve no local da injeção ou letargia transitória em doses supra-fisiológicas.
- Contraindicações: Deve-se evitar o uso em pacientes com neoplasias ativas devido ao potencial angiogênico (especialmente TB-500).
9 CONCLUSÕES
Os peptídeos biorreguladores e regenerativos representam a "chave molecular" para a medicina regenerativa veterinária. A integração do Renisamin no manejo da DRCF e do BPC-157/TB-500 na ortopedia permite resultados superiores às terapias convencionais isoladas. Esta monografia conclui que a padronização de protocolos e a educação continuada de médicos-veterinários são os próximos passos para a consolidação desta revolução terapêutica.
REFERÊNCIAS BIBLIOGRÁFICAS
ANISIMOV, V. N. Peptides and Cancer. Critical Reviews in Oncology/Hematology, v. 47, p. 145-156, 2003.
AMICHETTI, C. O Veterinário do Futuro e a Biologia Profunda. Petclube Archives, São Paulo, 1995.
GOLDSTEIN, A. L. et al. Thymosin β4: a multi-functional regenerative peptide. Basic & Clinical Pharmacology & Toxicology, v. 110, n. 1, p. 79-88, 2012.
KHAVINSON, V. K. Peptides and Regeneration. Gerontology, v. 48, n. 5, p. 267-271, 2002.
KHAVINSON, V. K.; MALININ, V. V. Peptide bioregulation of aging: results and prospects. Biogerontology, v. 6, p. 321-326, 2005.
RUSSIAN PEPTIDE. Тимозин-β4 или TB-500: Большой обзор. Disponível em: https://russianpeptide.com/timozin-4-ili-tb-500-bolshoj-obzor/. Acesso em: 08 mar. 2026.
SIKIRIC, P. et al. BPC 157 and Standard Angiogenic Factors. Current Pharmaceutical Design, v. 24, n. 21, p. 1-12, 2018.
WADA. World Anti-Doping Code International Standard Prohibited List 2024. Montreal: WADA, 2024.
XING, Y. et al. Progress on the function and application of thymosin β4. Frontiers in Endocrinology, v. 12, p. 767785, 2021.
XU, T. et al. Recombinant human thymosin β4 (NL005) in healthy volunteers: A randomized, double-blind, placebo-controlled phase I study. Peptides, v. 1, n. 2, p. 170574, 2021.
DISCLAIMER CIENTÍFICO
O TB-500, BPC 157 não possui aprovação como medicamento veterinário em diversas jurisdições internacionais, incluindo regulações supervisionadas pela European Medicines Agency dentro do regulamento Regulation (EU) 2019/6. Portanto: é frequentemente classificado como peptídeo de pesquisa; seu uso clínico formal não é aprovado em muitos países; qualquer aplicação deve ser considerada experimental ou off-label. Este conteúdo tem caráter exclusivamente científico e educacional, voltado à discussão de novas possibilidades em medicina regenerativa veterinária. Sempre respeite a legislação veterinária vigente e as normas do conselho profissional.
CITAÇÃO FINAL
"O veterinário do futuro não será apenas um prescritor de fármacos. Ele será um médico que entende biologia profunda, regeneração tecidual e medicina translacional." (AMICHETTI, 1995)
|
Característica |
TB-500 (Thymosin β-4 fragment) |
Peptídeos Biorreguladores Russos |
|---|---|---|
|
Origem |
Fragmento sintético do Thymosin β-4 natural |
Extratos peptídicos órgão-específicos (Khavinson, 1970s) |
|
Fonte Principal |
Produção sintética comercial (China, EUA) |
Instituto de Gerontologia de São Petersburgo, Rússia |
|
Especificidade |
Sistêmica — atua em múltiplos tecidos |
Órgão-específica — cada peptídeo targeting um órgão |
|
Mecanismo Principal |
Regulação de actina, angiogênese, migração celular |
Regulação epigenética, proteção mitocondrial, modulação imune |
|
Aplicações Veterinárias |
Ortopedia equina (tendões, ligamentos), cicatrização |
Gerontologia, nefrologia (Renisamin), neurologia (Cortexin) |
|
Status Regulatório |
Não aprovado — "research chemical" |
Alguns aprovados na Rússia (Cortexin, Thymalin) |
|
Evidência Científica |
Estudos pré-clínicos, uso experimental |
Ensaios clínicos russos, estudos de longevidade |
|
Dose Típica (Equinos) |
4-8 mg/semana (carga), 2-4 mg/manutenção |
Variável conforme peptídeo e espécie |
|
Via de Administração |
Subcutânea ou Intramuscular |
Subcutânea, Intramuscular, Oral (alguns) |
|
Foco Terapêutico |
Regeneração tecidual aguda (lesões) |
Rejuvenescimento celular, suporte órgão-específico |
|
Aplicação em Felinos |
Experimental — lesões ortopédicas |
Renisamin — potencial para IRC felina |
|
Aplicação em Caninos |
Ortopedia experimental, pós-cirúrgico |
Cortexin — neuroproteção, Livagen — hepático |
|
Riscos Conhecidos |
Aceleração tumoral dormente, falta de padronização |
Perfil de segurança estabelecido em estudos russos |
|
Controle Antidoping |
Proibido pela WADA (S2) |
Não listados especificamente |
|
Critério |
Peptídeos Biorreguladores |
Células-Tronco (MSCs) |
PRP (Plasma Rico em Plaquetas) |
|---|---|---|---|
|
Mecanismo de Ação |
Epigenética Direta: Modulação da metilação do DNA e acetilação de histonas |
Efeito Parácrino: Secreção de secretoma e vesículas extracelulares (EVs) |
Liberação de fatores de crescimento armazenados |
|
Eficácia em Ligamentos |
Alta (BPC-157/TB-500): angiogênese e organização de colágeno |
Robusta: redução de relesão (<28% em equinos) |
Moderada: ação limitada no tempo |
|
Eficácia na DRC |
Promissora: proteção tubular e redução de fibrose (Renisamin) |
Mista: melhora proteinúria, impacto inconsistente na TFG |
Baixa: pouca evidência para uso sistêmico |
|
Logística |
Baixa Complexidade: estáveis, liofilizados, baixo custo |
Alta Complexidade: cultivo, criopreservação, cadeia de frio |
Simples: centrifugação no local |
|
Barreiras Regulatórias |
Ambíguas: classificados como suplementos ou insumos |
Definidas: produtos de terapia avançada (ATMPs) |
Moderadas: procedimento autólogo |
|
Via de Sinalização |
Regulação transcricional direta (NF-κB, VEGF) |
Sinalização ambiental (TGF-β, IL-10) |
Receptores de superfície (PDGF, TGF-β) |
|
Custo Relativo |
Moderado |
Alto |
Baixo a Moderado |
|
Risco Imunológico |
Nulo (baixo peso molecular) |
Baixo a Moderado (autólogo vs. alogênico) |
Nulo (autólogo) |
|
Espécie |
Peptídeo Principal |
Indicação Clínica |
Protocolo Sugerido |
|---|---|---|---|
|
Cães |
BPC-157 + Cortexin |
Ortopedia e Disfunção Cognitiva |
BPC: 10-20mcg/kg/dia (SubQ); Cortexin: 5-10mg (IM) |
|
Gatos |
Renisamin + Vasalamin |
Doença Renal Crônica (DRCF) |
Renisamin: 10mg/dia; Vasalamin: 5mg/dia (ciclos de 10 dias) |
|
Equinos |
TB-500 + BPC-157 |
Lesões Tendíneas e Ligamentares |
TB-500: 4-8mg/semana (carga); BPC: 2-5mg/dia |
|
Aves |
Bronchogen |
Afecções Respiratórias Crônicas |
Nebulização ou via oral (dosagem ajustada por peso) |
|
Bovinos |
Livagen |
Recuperação Metabólica Pós-Parto |
Administração parenteral para suporte hepático |
|
Lagomorfos |
Epitalon |
Longevidade e suporte sistêmico |
Protocolos experimentais em desenvolvimento |
|
Peptídeo |
Órgão-Alvo |
Mecanismo de Ação |
Aplicação Veterinária |
|---|---|---|---|
|
Livagen |
Fígado |
Regeneração de hepatócitos, redução de fibrose |
Hepatopatias crônicas, suporte metabólico |
|
Renisamin |
Rins |
Proteção do epitélio tubular, modulação nitrogenada |
Doença Renal Crônica Felina (DRCF) |
|
Cortexin |
Cérebro |
Neuroproteção, plasticidade sináptica |
Disfunção Cognitiva Canina, epilepsia |
|
Retinalamin |
Retina |
Melhora microcirculação ocular, proteção fotoreceptores |
Degeneração retiniana, catarata senil |
|
Vasalamin |
Vasos Sanguíneos |
Estabilização endotelial, melhora microcirculação |
Doenças cardiovasculares, hipertensão |
|
Bronchogen |
Pulmões |
Regeneração epitelial pulmonar |
Afecções respiratórias crônicas |
|
Epitalon |
Glândula Pineal |
Regulação do ciclo sono-vigília, melatonina |
Gerontologia, distúrbios do sono |
|
Thymalin |
Timo |
Modulação imunológica, restauração timócitos |
Imunodeficiências, infecções recorrentes |
|
Característica |
TB-500 (fragmento de Timosina β-4) |
Peptídeos biorreguladores russos |
|---|---|---|
|
Origem |
Fragmento sintético de Timosina β-4 (Tβ4) natural |
Extratos/peptídeos órgão-específicos (escola russa; década de 1970) |
|
Fonte principal |
Produção sintética comercial (diversos países) |
Instituto de Bioregulação e Gerontologia de São Petersburgo (Rússia) |
|
Especificidade |
Sistêmica; múltiplos tecidos |
Órgão-específica; um peptídeo por órgão-alvo |
|
Mecanismo principal |
Regulação de actina, angiogênese, migração celular |
Regulação epigenética, proteção mitocondrial, modulação imune |
|
Aplicações veterinárias (exemplos) |
Ortopedia equina (tendões/ligamentos), cicatrização |
Gerontologia; nefrologia (Renisamin); neurologia (Cortexin) |
|
Status regulatório |
Não aprovado; frequentemente classificado como produto de pesquisa |
Alguns aprovados na Rússia (ex.: Cortexin, Thymalin) |
|
Evidência científica |
Predominantemente pré-clínica e uso experimental |
Ensaios clínicos russos e estudos de longevidade; heterogeneidade metodológica |
|
Dose típica (equinos) |
4–8 mg/semana (carga); 2–4 mg/semana (manutenção) |
Variável conforme peptídeo e espécie |
|
Via de administração |
Subcutânea ou intramuscular |
Subcutânea, intramuscular, oral (alguns) |
|
Foco terapêutico |
Regeneração tecidual aguda (lesões) |
Rejuvenescimento celular e suporte órgão-específico |
|
Aplicação em felinos |
Experimental; lesões ortopédicas |
Renisamin; potencial para DRC felina |
|
Aplicação em caninos |
Ortopedia experimental; pós-cirúrgico |
Cortexin (neuroproteção); Livagen (suporte hepático) |
|
Riscos/cautelas |
Variabilidade de padronização; cautela em contextos oncológicos |
Perfil de segurança descrito em estudos russos; requer validação por espécie/jurisdição |
|
Controle antidoping |
Proibido pela WADA (S2) |
Não listados especificamente |
|
Critério |
Peptídeos biorreguladores/regenerativos |
Células-tronco (MSCs) |
PRP (plasma rico em plaquetas) |
|---|---|---|---|
|
Mecanismo de ação |
Modulação molecular e transcricional; suporte mitocondrial; imunomodulação; alguns com hipótese epigenética |
Efeito parácrino (secretoma/EVs) e imunomodulação; potencial de diferenciação |
Liberação de fatores de crescimento e citocinas; modulação inflamatória local |
|
Eficácia em ligamentos |
Alta em modelos experimentais (ex.: BPC-157/TB-500); dependente de protocolo e padronização |
Robusta em parte da literatura (ex.: redução de relesão em equinos reportada em alguns estudos) |
Moderada; efeito geralmente limitado no tempo |
|
Eficácia na DRC |
Promissora (ex.: Renisamin como racional de proteção tubular e redução de fibrose) |
Mista; melhora de proteinúria com impacto inconsistente em TFG em diferentes estudos |
Baixa; pouca evidência para uso sistêmico |
|
Logística |
Baixa complexidade; estabilidade (liofilizados) e aplicação relativamente simples |
Alta complexidade; coleta, processamento/cultivo, criopreservação e cadeia de frio |
Simples; coleta e centrifugação no local |
|
Barreiras regulatórias |
Variáveis/ambíguas conforme país (suplemento, insumo de pesquisa, medicamento) |
Mais definidas e geralmente mais rigorosas (terapias avançadas/ATMPs) |
Moderadas; procedimento autólogo com regras locais |
|
Vias de sinalização (exemplos) |
Regulação transcricional e vias inflamatórias/angiogênicas (ex.: NF-κB, VEGF) |
Sinalização por citocinas/fatores (ex.: TGF-β, IL-10) e EVs |
Receptores ativados por fatores plaquetários (ex.: PDGF, TGF-β) |
|
Custo relativo |
Moderado |
Alto |
Baixo a moderado |
|
Risco imunológico |
Em geral baixo (peptídeos curtos), mas depende de pureza/formulação |
Baixo a moderado (autólogo vs. alogênico) e controle de qualidade |
Nulo (autólogo) |
|
Espécie |
Peptídeo(s) principal(is) |
Indicação clínica |
Protocolo sugerido (síntese) |
|---|---|---|---|
|
Cães |
BPC-157 + Cortexin |
Ortopedia e disfunção cognitiva |
BPC: 10–20 mcg/kg/dia (SC); Cortexin: 5–10 mg (IM) |
|
Gatos |
Renisamin + Vasalamin |
Doença renal crônica felina (DRCF) |
Renisamin: 10 mg/dia; Vasalamin: 5 mg/dia (ciclos de 10 dias) |
|
Equinos |
TB-500 + BPC-157 |
Lesões tendíneas e ligamentares |
TB-500: 4–8 mg/semana (carga); BPC: 2–5 mg/dia |
|
Aves |
Bronchogen |
Afecções respiratórias crônicas |
Nebulização ou via oral (ajuste por peso) |
|
Bovinos |
Livagen |
Recuperação metabólica pós-parto |
Administração parenteral para suporte hepático |
|
Lagomorfos |
Epitalon |
Longevidade e suporte sistêmico |
Protocolos experimentais em desenvolvimento |
|
Peptídeo |
Órgão-alvo |
Mecanismo de ação (síntese) |
Aplicação veterinária (exemplos) |
|---|---|---|---|
|
Livagen |
Fígado |
Regeneração de hepatócitos; redução de fibrose |
Hepatopatias crônicas; suporte metabólico |
|
Renisamin |
Rins |
Proteção do epitélio tubular; modulação nitrogenada |
DRC felina (potencial); suporte renal |
|
Cortexin |
Cérebro |
Neuroproteção; plasticidade sináptica |
Disfunção cognitiva canina; epilepsia |
|
Retinalamin |
Retina |
Microcirculação ocular; proteção de fotorreceptores |
Degeneração retiniana; catarata senil |
|
Vasalamin |
Vasos sanguíneos |
Estabilização endotelial; melhora de microcirculação |
Doenças cardiovasculares; hipertensão |
|
Bronchogen |
Pulmões |
Regeneração epitelial pulmonar |
Afecções respiratórias crônicas |
|
Epitalon |
Glândula pineal |
Regulação sono-vigília; melatonina |
Gerontologia; distúrbios do sono |
|
Thymalin |
Timo |
Modulação imunológica; suporte a timócitos |
Imunodeficiências; infecções recorrentes |
|
Condição clínica |
Peptídeo(s) sugerido(s) |
Órgão/Sistema-alvo |
Potencial terapêutico |
Fase de aplicação |
|---|---|---|---|---|
|
Disfunção cognitiva canina (DCC) |
Cortexin; Endoluten |
Cérebro; glândula pineal |
Alto |
Médio a longo prazo |
|
Osteoartrite e doença articular degenerativa |
BPC-157; TB-500; Cartalax |
Articulações; cartilagem; tecidos moles |
Alto |
Curto a longo prazo |
|
Ruptura de ligamento cruzado cranial (pós-cirúrgico) |
BPC-157; TB-500 |
Ligamentos; tecidos moles |
Alto |
Curto a médio prazo |
|
Mielopatia degenerativa |
Cortexin; BPC-157 |
Medula espinhal; nervos |
Moderado |
Médio a longo prazo |
|
Hepatopatias crônicas |
Livagen |
Fígado |
Alto |
Médio a longo prazo |
|
Doença renal crônica |
Renisamin |
Rins |
Alto |
Médio a longo prazo |
|
Dermatites e cicatrização de feridas |
GHK-Cu; BPC-157 |
Pele; tecido conjuntivo |
Alto |
Curto a médio prazo |
|
Condição clínica |
Peptídeo(s) sugerido(s) |
Órgão/Sistema-alvo |
Potencial terapêutico |
Fase de aplicação |
|---|---|---|---|---|
|
Doença renal crônica felina (DRCF) |
Renisamin |
Rins |
Alto |
Médio a longo prazo |
|
Asma felina e bronquite crônica |
Bronchogen |
Pulmões; brônquios |
Moderado |
Médio prazo |
|
Hepatopatias (ex.: lipidose hepática) |
Livagen |
Fígado |
Moderado a alto |
Médio prazo |
|
Estomatite crônica felina |
Thymalin; BPC-157 |
Sistema imune; mucosa oral |
Moderado |
Curto a médio prazo |
|
Osteoartrite em gatos idosos |
BPC-157; Cartalax |
Articulações; cartilagem |
Moderado a alto |
Curto a longo prazo |
|
Retinopatias degenerativas |
Retinalamin |
Retina |
Moderado |
Médio a longo prazo |
|
Condição clínica |
Peptídeo(s) sugerido(s) |
Órgão/Sistema-alvo |
Potencial terapêutico |
Fase de aplicação |
|---|---|---|---|---|
|
Tendinopatias e lesões de ligamentos (ex.: TFDS) |
TB-500; BPC-157 |
Tendões; ligamentos |
Alto |
Curto a médio prazo |
|
Osteoartrite e doença articular degenerativa |
BPC-157; Cartalax |
Articulações; cartilagem |
Alto |
Médio a longo prazo |
|
Laminite crônica |
BPC-157; Vasalamin |
Lâminas do casco; vasos sanguíneos |
Moderado |
Médio prazo |
|
Úlceras gástricas |
BPC-157 |
Mucosa gástrica |
Alto |
Curto a médio prazo |
|
Miopatias de esforço |
TB-500; BPC-157 |
Músculos |
Moderado |
Curto a médio prazo |
Disclaimer Informativo sobre Peptídeos Bioreguladores em Medicina Veterinária
Dr. Cláudio Amichetti Júnior
Médico Veterinário
CRMV-SP 75.404 VT | MAPA 00129461/2025 | CREA 060149829-SP
Medicina Integrativa, Nutrição Felina e Canina, Medicina Canabinoide
Petclube - São Paulo, SP
Declaração de Orientação Informativa e Não Prescritiva
Eu, Dr. Cláudio Amichetti Júnior, médico veterinário devidamente registrado no CRMV-SP sob o nº 75.404 VT, venho por meio deste fornecer orientação informativa e educacional sobre o uso de peptídeos bioreguladores (ex.: BPC-157, TB-500 ou similares).
Contexto Científico:
- Os peptídeos bioreguladores são compostos promissores em estudos pré-clínicos, in vitro e relatos clínicos iniciais.
- Ainda estão em fase experimental, sem aprovação plena pela ANVISA ou regulamentação específica pelo MAPApara uso rotineiro em veterinária no Brasil.
- Não existem protocolos consolidados, e os resultados variam conforme o animal, dosagem e contexto clínico.
Escopo da Orientação:
Esta comunicação é puramente informativa e educacional. Forneço sugestões baseadas em evidências científicas disponíveis (estudos animais, relatos e literatura), incluindo:
- Doses referenciais.
- Vias de administração.
- Possíveis combinações.
Não se trata de:
- Prescrição médica veterinária.
- Diagnóstico.
- Tratamento oficial ou endossado.
- Recomendação para uso imediato.
Responsabilidades:
- Recomendo consultar um veterinário de sua confiança para avaliação individualizada do animal, incluindo exames complementares.
- Qualquer aplicação deve ser feita sob supervisão profissional, com produtos de fontes confiáveis, testes laboratoriais prévios e monitoramento contínuo.
- A decisão de uso é de sua exclusiva responsabilidade. Eu me reservo o direito de não endossar aplicações sem dados clínicos completos.
Base Ética e Legal:
De acordo com o Código de Ética do CRMV-SP (Resolução nº 1.228/2018) e normas do Conselho Federal de Medicina Veterinária (CFMV):
- Priorizo o bem-estar animal e a ciência baseada em evidências.
- Terapias experimentais devem seguir princípios éticos, com consentimento informado e monitoramento.
Em caso de dúvidas ou intercorrências, contate o CRMV-SP ou um profissional registrado.
Atenciosamente,
Dr. Cláudio Amichetti Júnior
CRMV-SP 75.404 VT
Contato: dr.claudio.amichetti@gmail.com
A Composição Lipídica das Membranas e a Longevidade Felina: Ferroptose, Peroxidação Lipídica, mTOR/AMPK e Implicações Pancreáticas e Hepáticas
Cláudio Amichetti Júnior¹,²
Gabriel Amichetti³
¹ Médico-veterinário Integrativo – CRMV-SP 75.404 VT; CREA 060149829-SP
² [Afiliação Institucional Petclube, São Paulo, Brasil]
³ Médico-veterinário, Especialização em Ortopedia e Cirurgia de Pequenos Animais-CRMV-SP 45592 VT– [clínica 3RD Vila Zelina SP]
Autor Correspondente: Cláudio Amichetti Júnior, [dr.claudio.amichetti@gmail.com]
Resumo
A composição dos ácidos graxos nas membranas celulares determina a fluidez, a susceptibilidade à oxidação e a interação com vias de sinalização (mTOR, AMPK) que regulam envelhecimento, autofagia e função mitocondrial. Em felinos, cuja fisiologia lipídica é particular (dependência exógena de ARA/EPA/DHA e menor atividade de desaturases), a desregulação do perfil de membrana está associada a peroxidação lipídica, ferroptose e disfunção das células β pancreáticas — contribuindo para resistência à insulina, esteatose hepática e progressão para diabetes mellitus. Ácidos graxos saturados de cadeia ímpar (p.ex. pentadecanoico, C15:0) emergem como lipídios estruturais capazes de aumentar a estabilidade das membranas, ativar AMPK e inibir mTOR, reduzindo estresse oxidativo e vulnerabilidade à ferroptose. Este artigo revisa mecanisticamente esses pontos com foco clínico-veterinário para gatos, resumindo evidências experimentais e recomendações nutricionais e de pesquisa. O papel da alimentação natural, em particular do peixe como fonte de C15, é destacado em contraste com dietas comerciais ricas em carboidratos. A imperiosa necessidade de ensaios clínicos randomizados e cegos em populações felinas diversas é enfatizada para a validação destas intervenções.
Palavras-chave: felinos; ferroptose; C15:0; mTOR; AMPK; resistência à insulina; esteatose hepática; nutrição veterinária; longevidade.
Abstract (English)
The fatty acid composition of cell membranes determines fluidity, susceptibility to oxidation, and interaction with signaling pathways (mTOR, AMPK) that regulate aging, autophagy, and mitochondrial function. In felines, whose lipid physiology is particular (exogenous dependence on ARA/EPA/DHA and lower desaturase activity), membrane profile dysregulation is associated with lipid peroxidation, ferroptosis, and pancreatic β-cell dysfunction – contributing to insulin resistance, hepatic steatosis, and progression to diabetes mellitus. Odd-chain saturated fatty acids (e.g., pentadecanoic acid, C15:0) emerge as structural lipids capable of increasing membrane stability, activating AMPK, and inhibiting mTOR, thereby reducing oxidative stress and susceptibility to ferroptosis. This article mechanistically reviews these points with a clinical-veterinary focus on cats, summarizing experimental evidence and nutritional and research recommendations. The role of natural feeding, particularly fish as a source of C15, is highlighted in contrast to carbohydrate-rich commercial diets. The imperative need for randomized, blinded clinical trials in diverse feline populations is emphasized for the validation of these interventions.
Keywords: felines; ferroptosis; C15:0; mTOR; AMPK; insulin resistance; hepatic steatosis; veterinary nutrition; longevity.
1. Introdução
A longevidade e a saúde de um organismo multicelular são intrinsecamente ligadas à capacidade de suas células em manter a integridade estrutural e funcional de suas membranas biológicas frente a um constante bombardeio de estresses ambientais e metabólicos. Essas bicamadas lipídicas, longe de serem meras barreiras passivas, são plataformas dinâmicas que orquestram a sinalização celular, o transporte de nutrientes e a defesa contra o estresse oxidativo [1]. Na medicina veterinária contemporânea, a crescente prevalência de doenças metabólicas crônicas em animais de companhia – como o diabetes mellitus tipo 2, a pancreatite e a esteatose hepática – representa um desafio significativo e uma prioridade de pesquisa urgente, especialmente em felinos, uma espécie com fisiologia metabólica singular e alta suscetibilidade a tais condições.
Felinos, como carnívoros estritos, possuem um metabolismo otimizado para a utilização de proteínas e gorduras, e uma capacidade limitada de processar carboidratos [2]. Essa particularidade os torna metabolicamente vulneráveis a dietas comerciais formuladas com altas concentrações de carboidratos, frequentemente convertidos em gordura hepática (lipogênese de novo), culminando em resistência à insulina e esteatose hepática [3]. A desregulação da composição lipídica das membranas celulares, exacerbada por esses perfis dietéticos, predispõe à peroxidação lipídica e à ferroptose – uma forma programada de morte celular dependente de ferro e estresse oxidativo lipídico [4,5]. Paralelamente, vias de sinalização críticas como o mTOR (mammalian Target of Rapamycin) e a AMPK (AMP-activated protein kinase) orquestram a resposta celular à disponibilidade de nutrientes e energia, e sua desregulação contribui para o ciclo vicioso de inflamação crônica, disfunção mitocondrial e progressão da doença [6,7].
Este artigo se propõe a desvendar as complexas interações moleculares que conectam a saúde das membranas lipídicas à homeostase metabólica e à longevidade em felinos. Exploraremos como a arquitetura lipídica das membranas celulares influencia criticamente a sinalização mTOR/AMPK e a ferroptose. Analisaremos o impacto deletério das dietas comerciais ricas em carboidratos na etiologia da esteatose hepática e na resistência à insulina em gatos, contrastando com o potencial terapêutico de uma alimentação natural e a importância de lipídios bioativos, como o ácido pentadecanoico (C15:0), encontrado em fontes como o peixe [8]. Para embasar essa perspectiva, integraremos insights de modelos comparativos excepcionais, como os golfinhos da Marinha dos EUA, que exibem notável flexibilidade metabólica e longevidade celular [9], e as inovações em lipídios de cadeia ímpar desenvolvidas pela Seraphina Therapeutics [10], bem como as contribuições teóricas de Sthefany Von Whatson sobre bioenergética mitocondrial [11]. O objetivo é fornecer uma compreensão aprofundada dos mecanismos subjacentes a essas doenças e propor estratégias nutricionais e terapêuticas inovadoras, pautadas na biologia felina. Contudo, é fundamental ressaltar que a translação dessas descobertas para a prática clínica veterinária exige um rigor científico incontestável, reiterando a necessidade premente de estudos duplos-cegos, randomizados e controlados em diversas populações felinas para validar plenamente estas abordagens.
2. Bases Bioquímicas: Membrana, Espécies Reativas e Peroxidação Lipídica
2.1 Composição da Membrana e Suscetibilidade à Oxidação
A bicamada lipídica das membranas celulares é composta por fosfolipídios, glicolipídios e colesterol, nos quais ácidos graxos saturados, monoinsaturados e poli-insaturados (PUFAs) estão esterificados. A proporção e o tipo de ácidos graxos incorporados nas membranas são cruciais para sua fluidez, permeabilidade e a atividade de proteínas de membrana, incluindo receptores e enzimas [12]. A presença elevada de PUFAs, especialmente os de cadeia longa e alta insaturação (como o ácido araquidônico – ARA, eicosapentaenoico – EPA e docosahexaenoico – DHA), aumenta a probabilidade de formação de lipoperóxidos quando confrontados com Espécies Reativas de Oxigênio (EROs) ou Nitrogênio (ERNs). Gatos, em particular, têm uma dependência dietética de ARA, EPA e DHA devido à baixa atividade das enzimas delta-6-desaturase e delta-5-desaturase, o que os torna especialmente sensíveis à qualidade e tipo de lipídios na dieta [2].
2.2 Mecanismos de Peroxidação Lipídica
A peroxidação lipídica é um processo radicalar em cadeia que envolve a oxidação de PUFAs nas membranas. Inicia-se pela abstração de um átomo de hidrogênio de um PUFA por um radical livre, formando um radical lipídico (L•). Este radical reage com oxigênio molecular para formar um radical peroxil lipídico (LOO•), que pode abstrair um hidrogênio de outro PUFA, propagando a reação em cadeia e gerando um hidroperóxido lipídico (LOOH). A falha das defesas antioxidantes, como o sistema Glutationa (GSH)/Glutationa Peroxidase 4 (GPX4) e antioxidantes lipofílicos (e.g., Vitamina E), culmina no acúmulo de lipídios oxidados. Produtos secundários altamente reativos, como o malondialdeído (MDA) e o 4-hidroxinonenal (4-HNE), podem carbonilar proteínas, lipídios e DNA, comprometendo a função de bombas iônicas e canais de membrana. Isso é particularmente danoso em células sensíveis, como as células β pancreáticas, prejudicando a secreção insulínica e a homeostase metabólica [5,13].
3. Ferroptose: Definição, Marcadores Moleculares e Relevância para o Pâncreas e Fígado Felino
3.1 Características Distintivas da Ferroptose
Ferroptose é uma forma de morte celular regulada distinta da apoptose e da necrose, caracterizada por sua dependência de ferro e peroxidação de fosfolipídios [4,5]. Seus marcadores bioquímicos incluem a inibição da atividade da GPX4, o consumo de GSH e o acúmulo massivo de peróxidos de fosfolipídios. Morfologicamente, mitocôndrias de células em ferroptose frequentemente exibem diminuição do volume, densidade aumentada da membrana externa, cristalização das cristas mitocondriais e perda do potencial de membrana mitocondrial [14].
3.2 Vulnerabilidade das Ilhotas Pancreáticas e Hepatócitos Felinos
As células β pancreáticas são notoriamente vulneráveis ao estresse oxidativo devido à sua baixa expressão de enzimas antioxidantes e alta atividade metabólica. Em felinos obesos e insulinorresistentes, a peroxidação lipídica e a ferroptose desempenham um papel crítico na progressão da doença. Observa-se nessas condições o acúmulo lipídico intra-ilhotas, estresse do retículo endoplasmático (ER) e aumento de EROs, criando um ambiente pro-ferroptótico. Isso leva à perda funcional das células β, acelerando a progressão para a falência permanente da secreção de insulina e o desenvolvimento de diabetes mellitus [15]. Clinicamente, a ferroptose nessas células contribui para a menor taxa de remissão do diabetes em felinos quando comparado a intervenções precoces.
No contexto hepático, a esteatose felina (fígado gorduroso) é outra condição onde a ferroptose é uma preocupação significativa. O acúmulo excessivo de triglicerídeos nos hepatócitos predispõe o fígado a um estado de estresse oxidativo crônico e inflamação, aumentando a suscetibilidade à peroxidação lipídica e, consequentemente, à ferroptose dos hepatócitos. Este mecanismo contribui para a progressão do dano hepático e pode levar à insuficiência hepática aguda [3]. A compreensão desses mecanismos é crucial para o desenvolvimento de terapias protetoras, incluindo as que visam a resiliência tecidual em cenários de lesão aguda ou estresse cirúrgico (conforme observado por Gabriel Amichetti), onde a liberação de ferro e o estresse oxidativo podem exacerbar o dano celular e comprometer a recuperação.
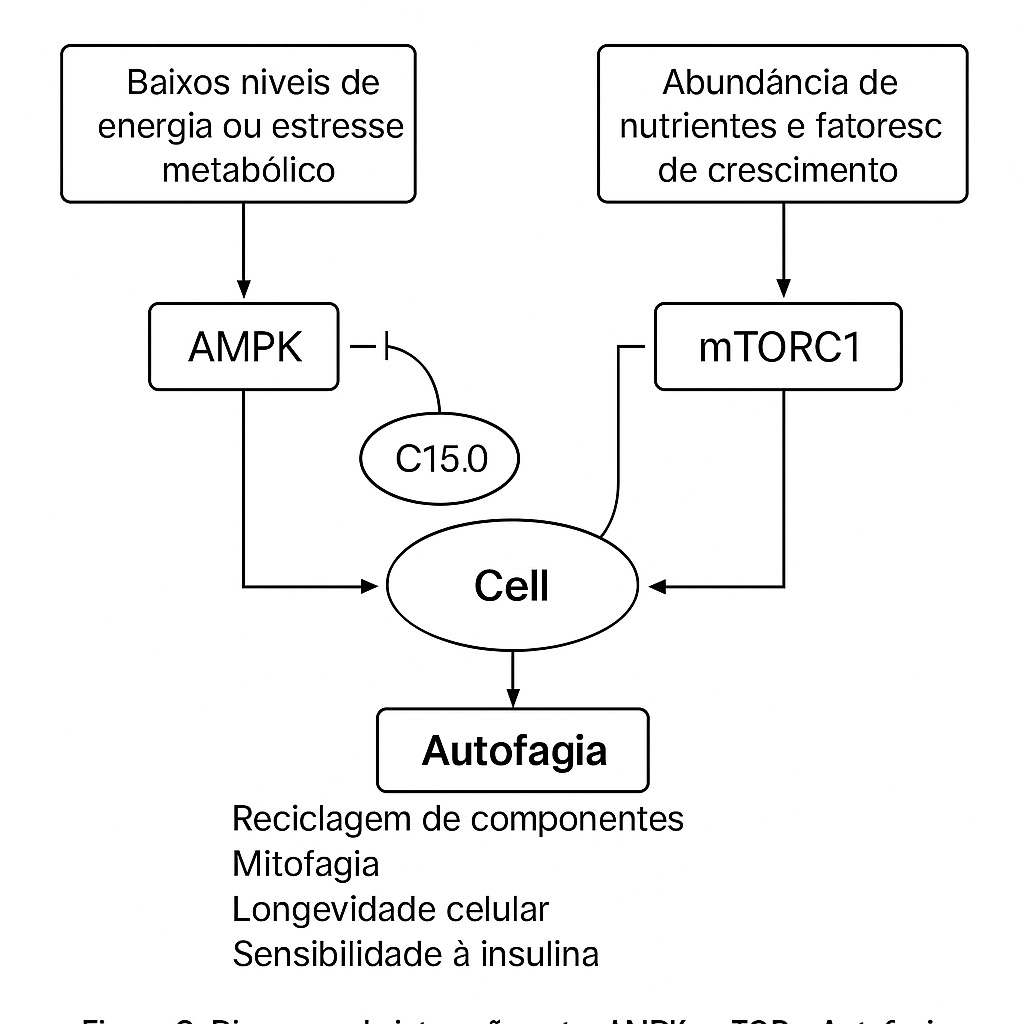
4. mTOR / AMPK: Integração Energética, Autofagia e Relação com Lipídios de Membrana
4.1 Papel Central do mTORC1 e Efeitos de Sua Hiperatividade
O complexo mTORC1 (mammalian Target of Rapamycin Complex 1) é um sensor central de nutrientes e energia, integrando sinais de aminoácidos, glicose e insulina para promover o crescimento celular, a síntese proteica e o anabolismo [6,16]. Em condições de excesso nutricional, a hiperatividade crônica do mTORC1 tem sido associada à resistência à insulina, pois pode levar à fosforilação inibitória de substratos do receptor de insulina (IRS-1), prejudicando a sinalização da insulina [7]. Além disso, a ativação excessiva do mTORC1 inibe a autofagia, um processo essencial de degradação e reciclagem de componentes celulares danificados, incluindo mitocôndrias (mitofagia). O acúmulo de mitocôndrias disfuncionais contribui para o aumento de EROs e o estresse oxidativo, fechando um ciclo vicioso que agrava o dano celular e a disfunção metabólica [17].
4.2 Ativação de AMPK como Contraponto Protetor
A AMPK (AMP-activated protein kinase) atua como um sensor de baixo estado energético celular. Quando ativada (e.g., por elevações na razão AMP:ATP), a AMPK estimula processos catabólicos para gerar energia, como a oxidação de ácidos graxos, e inibe vias anabólicas, incluindo a via mTORC1 [18]. A ativação da AMPK promove a autofagia, favorecendo a eliminação de mitocôndrias danificadas e a redução de EROs. Muitos moduladores metabólicos benéficos, como a restrição calórica e a metformina, exercem seus efeitos terapêuticos, em parte, através da ativação da AMPK.
4.3 Lipídios Estruturais Modulam Essas Vias
A composição lipídica das membranas celulares pode modular diretamente a atividade de proteínas sinalizadoras como mTOR e AMPK. A fluidez da membrana, determinada pela proporção de ácidos graxos saturados, monoinsaturados e poli-insaturados, afeta a formação de microdomínios lipídicos ("rafts") e a localização funcional de receptores e complexos sinalizadores. Lipídios oxidáveis, ao induzir estresse oxidativo e inflamação, podem favorecer a hiperatividade de vias pró-senescência e inflamatórias. Em contraste, lipídios estruturais mais estáveis, como os ácidos graxos saturados de cadeia ímpar, podem promover um estado pró-reparo e de homeostase. Estudos emergentes demonstram que o ácido pentadecanoico (C15:0) pode ativar a AMPK e inibir o mTOR em modelos celulares e animais, sugerindo um papel na otimização da sinalização energética celular e na promoção da autofagia [8,10].
5. Golfinhos da Marinha Norte-Americana como Modelo Comparativo para a Medicina Veterinária Felina
O programa de mamíferos marinhos da Marinha dos EUA (U.S. Navy Marine Mammal Program) revelou um fenômeno fisiológico notável em golfinhos: a capacidade de alternar entre estados de resistência e sensibilidade à insulina pós-prandial e, em seguida, retornar rapidamente a um estado de normossensibilidade, sem o dano pancreático ou hepático observado em outras espécies [9]. Este mecanismo de "diabetes reversível", mediado por uma flexibilidade metabólica excepcional, é de extremo interesse para a medicina veterinária.
Características celulares e metabólicas desses animais, que contribuem para sua resiliência, incluem:
- membranas altamente resistentes à oxidação, com perfis lipídicos favoráveis;
- eficiência mitocondrial excepcional, otimizando a produção de energia;
- baixa vulnerabilidade à ferroptose, protegendo os tecidos de danos;
- modulação natural e eficaz das vias mTOR e AMPK, sensores de energia cruciais;
- envelhecimento celular excepcionalmente lento, refletindo a proteção contra danos cumulativos.
Para felinos, este modelo inspirador de "adaptabilidade metabólica" impulsiona pesquisas sobre a reversão da resistência à insulina e a proteção pancreática e hepática. Assim como os golfinhos adaptam seu metabolismo a desafios ambientais, os gatos podem se beneficiar de estratégias que promovam maior flexibilidade metabólica, como a modulação da frequência alimentar (e.g., jejum intermitente adaptado) e a otimização da composição dietética, visando mimetizar respostas adaptativas naturais. A capacidade de um metabolismo flexível, que transita eficientemente entre o uso de carboidratos e gorduras, pode ser crucial para prevenir e reverter doenças metabólicas em felinos, incluindo a capacidade de mobilizar gordura do fígado de forma eficaz e sem toxicidade. Essas descobertas fornecem um pano de fundo para a contribuição teórica de Sthefany Von Whatson [11], que propõe que a estabilidade da membrana interna mitocondrial – e a composição lipídica da cardiolipina – é determinante para a eficiência da cadeia respiratória e a sensibilidade ao estresse oxidativo, impactando a vulnerabilidade à ferroptose e, em última instância, a longevidade celular.
6. Ácido Pentadecanoico (C15:0) e Lipídios Bioativos na Veterinária
6.1 Propriedades Benéficas do C15:0
O ácido pentadecanoico (FA15, também conhecido como C15:0), um ácido graxo saturado de cadeia ímpar, tem demonstrado uma gama de efeitos pleiotrópicos benéficos [8,10]:
- Ativação da AMPK: Um sensor de energia que promove o catabolismo e a autofagia;
- Inibição de mTOR: Reduzindo a hiperatividade associada à resistência à insulina e envelhecimento;
- Redução de inflamação sistêmica: Contribuindo para a resolução de estados inflamatórios crônicos de baixo grau;
- Aumento da autofagia: Processo essencial de reciclagem celular que remove organelas danificadas;
- Proteção mitocondrial: Melhorando a função e integridade das mitocôndrias;
- Menor peroxidação lipídica: Aumentando a resistência das membranas ao estresse oxidativo;
- Modulação imune: Contribuindo para a homeostase do sistema imunológico.
Estudos sugerem que o C15:0 pode atuar como um "lipídio sinalizador" que otimiza as vias metabólicas, promovendo a autofagia e a sensibilidade à insulina. Sua ação na estabilização de membranas e na modulação de vias metabólicas também confere um papel protetor ao fígado, auxiliando na prevenção e reversão da esteatose ao otimizar o metabolismo lipídico hepático [10].
6.2 Seraphina Therapeutics e Lipídios de Cadeia Ímpar
A Seraphina Therapeutics, pioneira em lipídios de cadeia ímpar, tem desenvolvido moléculas com potenciais aplicações veterinárias que visam promover o envelhecimento saudável, otimizar a saúde metabólica, favorecer a recuperação mitocondrial, oferecer suporte hepático contra doenças como a esteatose e modular doenças inflamatórias [10]. Essas moléculas, por sua estrutura saturada e de cadeia ímpar, resistem fortemente à oxidação, o que reduz a ativação de ferroptose em tecidos vulneráveis [8]. O C15:0 (FA15) é encontrado naturalmente em pequenas quantidades em gorduras lácteas e, significativamente para felinos, em certos peixes [10]. Em felinos, a inclusão dietética de fontes naturais de C15:0, como o peixe, pode atuar como um "protetor metabólico" crucial.
7. Implicações Metabólicas, Hepáticas e Terapêuticas em Medicina Veterinária
7.1 Pâncreas, Fígado e Resistência à Insulina: O Ciclo Patológico em Felinos e o Papel da Dieta Comercial
O metabolismo do felino, como carnívoro estrito, é intrinsecamente adaptado para dietas ricas em proteínas e gorduras, com uma capacidade limitada de processar grandes quantidades de carboidratos. Este fato tem implicações profundas na etiologia das doenças metabólicas.
- Dietas comerciais inadequadas, ricas em carboidratos: Quando felinos consomem rações comerciais com alto teor de carboidratos (muitas vezes necessários para a extrusão e formato do kibble), o excesso de glicose não pode ser eficientemente utilizado ou armazenado como glicogênio. Este excesso é então rapidamente convertido em gordura no fígado (lipogênese de novo).
- Acúmulo de gordura no fígado (Esteatose Hepática): Este processo sobrecarrega o metabolismo hepático, levando à acumulação de triglicerídeos nos hepatócitos. A esteatose hepática felina, em sua forma aguda ou crônica, é uma condição grave e potencialmente fatal, onde o fígado perde sua capacidade funcional [3].
- Resistência à insulina e hiperinsulinemia compensatória: O fígado gorduroso, juntamente com a disfunção pancreática, retroalimenta a resistência à insulina nos tecidos periféricos. Isso leva o pâncreas a secretar ainda mais insulina (hiperinsulinemia) na tentativa de normalizar a glicemia.
- Hiperatividade crônica do mTORC1: Exacerbada por dietas de alta energia e processadas, essa hiperatividade nas células β pancreáticas e nos hepatócitos bloqueia a autofagia, um processo vital de "limpeza" celular, e leva ao acúmulo de organelas danificadas.
- Aumento de EROs e estresse oxidativo: O acúmulo de mitocôndrias danificadas, devido à falta de autofagia e ao estresse metabólico contínuo, resulta em um aumento massivo de Espécies Reativas de Oxigênio (EROs) e estresse oxidativo no pâncreas e fígado [17].
- Oxidação lipídica descontrolada e ativação da ferroptose: A abundância de PUFAs nas membranas (muitas vezes proveniente de óleos vegetais em rações comerciais), combinada com o estresse oxidativo, leva à oxidação lipídica descontrolada. Este processo ativa a ferroptose nas células β e nos hepatócitos [3,5].
- Morte das células β e dano hepático progressivo: A ferroptose e outros mecanismos de morte celular resultam na redução progressiva da capacidade das células β de secretar insulina e no comprometimento irreversível da função hepática.
- Aumento glicêmico persistente e falha orgânica: Este ciclo culmina no agravamento do quadro metabólico, com desenvolvimento de diabetes mellitus, insuficiência hepática e esteatose hepática severa, comprometendo severamente a qualidade de vida e a longevidade do felino.
Lipídios estruturais estáveis, como o C15:0, podem modular esse dano, promovendo uma maior resiliência celular e interrompendo o ciclo patológico.
7.2 Nutrição Veterinária Orientada à Longevidade e à Resolução Metabólica: O Papel da Alimentação Natural e do Peixe
Considerando a complexidade desses mecanismos e o papel central da dieta, abordagens terapêuticas integrativas para felinos devem focar na otimização nutricional como pilar:
- Modulação Nutricional e Alimentação Natural como Pilar Terapêutico:
- Transição para dietas naturais, baseadas em carne, com baixo carboidrato e balanceadas em gorduras: Dietas formuladas para carnívoros estritos promovem uma melhor regulação da glicemia, reduzem o estresse pancreático e diminuem drasticamente a sobrecarga hepática por lipogênese de novo, prevenindo e auxiliando na reversão da esteatose hepática.
- Uso estratégico de peixe como fonte de lipídios benéficos e C15 (FA15): Certos peixes (e.g., salmão, sardinha, arenque), além de serem uma excelente fonte de proteínas de alta qualidade e ácidos graxos ômega-3 (anti-inflamatórios), podem fornecer o ácido pentadecanoico (FA15/C15). O FA15 atua na estabilização de membranas, proteção contra peroxidação lipídica e modulação de vias metabólicas como mTOR e AMPK, contribuindo para a sensibilidade à insulina, a resiliência celular e a saúde hepática, otimizando o metabolismo lipídico [8].
- Evitar rações comerciais processadas e desequilibradas: Que, devido ao seu alto teor de carboidratos e perfil lipídico inadequado, podem promover hiperatividade do mTORC1, estresse oxidativo, inflamação crônica e, crucialmente, a esteatose hepática, acelerando o ciclo patológico da resistência à insulina e ferroptose.
- Suplementação estratégica de ácidos graxos de cadeia ímpar (C15:0): Em casos onde a dieta não oferece quantidades suficientes ou há necessidades aumentadas, como em animais convalescentes ou com patologias específicas.
- Redução do excesso de PUFAs oxidáveis: Ajustando o perfil lipídico da dieta e a escolha de óleos e gorduras, priorizando fontes estáveis e com bom balanço ômega-3:ômega-6.
- Antioxidantes mitocondriais: Direcionados especificamente às mitocôndrias para combater EROs e proteger contra danos oxidativos no pâncreas e fígado (e.g., Coenzima Q10, Vitamina E).
- Modulação de mTOR e AMPK: Através de nutrientes e, se necessário, terapias específicas.
- Dietas com menor potencial pró-ferroptótico: Em gatos renais, cães geriátricos e animais com doenças hepáticas ou pancreáticas.
- Estímulos metabólicos adaptativos: Inspirados em mamíferos marinhos, visando aprimorar a flexibilidade metabólica e a resiliência das células β e dos hepatócitos.
| Componente | Recomendação % MS (Matéria Seca) | Justificativa |
|---|---|---|
| Proteína | > 40% | Essencial para carnívoros estritos, manutenção muscular, baixa carga glicêmica. |
| Gordura Total | 30-40% | Fonte primária de energia, transporte de vitaminas lipossolúveis. |
| Carboidratos (NFE) | < 10% | Mínimo necessário, felinos possuem baixa capacidade de metabolização de carboidratos. |
| Fibra | ~ 5% | Saúde gastrointestinal, controle glicêmico. |
| Ácidos Graxos Ômega-3 (EPA/DHA) | Proporção adequada | Anti-inflamatório, saúde cerebral e de pele, balanço com ômega-6. |
| C15:0 (Ácido Pentadecanoico) | Presente em fontes naturais | Lipídio estrutural de membrana, modula AMPK/mTOR, proteção contra ferroptose. |
| Antioxidantes (Vitamina E, Taurina) | Níveis adequados | Proteção celular contra EROs, suporte hepático e cardíaco. |
7.3 Necessidade de Pesquisas Rigorosas em Felinos
Embora a compreensão dos mecanismos celulares e os insights de modelos comparativos e novos lipídios bioativos sejam promissores, a aplicação prática dessas estratégias na medicina veterinária requer validação científica robusta. É imperativa a realização de estudos duplos-cegos, randomizados e controlados, com diferentes grupos de felinos, incluindo animais saudáveis, com sobrepeso, diabéticos e aqueles com diagnóstico de esteatose hepática. Tais estudos devem visar:
- Confirmar a eficácia e segurança da alimentação natural e da suplementação com C15:0 (FA15) em diversos cenários clínicos.
- Comparar objetivamente os desfechos metabólicos e clínicos de dietas naturais versus dietas comerciais formuladas, avaliando parâmetros como sensibilidade à insulina, marcadores de estresse oxidativo, função hepática e pancreática, e composição corporal.
- Determinar dosagens ótimas e avaliar os efeitos a longo prazo das intervenções dietéticas e nutracêuticas em diferentes grupos etários e condições patológicas.
- Investigar a modulação de biomarcadores de mTOR, ferroptose, estresse oxidativo e saúde mitocondrial em resposta às intervenções de forma precisa.
A medicina veterinária baseada em evidências depende desses estudos para guiar as melhores práticas clínicas e oferecer as mais eficazes e seguras opções terapêuticas aos pacientes felinos.
8. Considerações Éticas e de Segurança
Até que existam dados robustos e específicos em felinos, qualquer intervenção nutricional ou suplementação, especialmente com novos compostos bioativos, deve ser conduzida sob rigoroso protocolo aprovado por comitê de ética e com monitorização contínua de parâmetros clínicos, bioquímicos (hepáticos, renais, perfil lipídico) e de segurança. Doses extrapoladas de outras espécies, incluindo humanos, não são automaticamente seguras ou eficazes para gatos. Intervenções dietéticas devem sempre respeitar as necessidades nutricionais específicas e inflexíveis dos felinos (e.g., taurina, arginina, Vitamina A pré-formada), para evitar deficiências e toxicidades.
9. Conclusão
A composição lipídica das membranas celulares emerge como um fator determinante e muitas vezes negligenciado para o envelhecimento, a função mitocondrial e a homeostase metabólica em medicina veterinária. Lipídios estáveis, notavelmente o C15:0, promovem uma maior longevidade celular e proteção intrínseca contra mecanismos deletérios como a ferroptose, enquanto um excesso de PUFAs oxidáveis pode acelerar a peroxidação lipídica e o dano tecidual. Modelos comparativos como os golfinhos, pesquisas inovadoras da Seraphina Therapeutics e as teorias de bioenergética de Sthefany Von Whatson oferecem uma moldura conceitual rica para o entendimento moderno do envelhecimento e da disfunção metabólica em animais.
A relação direta entre dietas comerciais ricas em carboidratos e a patogênese da esteatose hepática felina, juntamente com a resistência à insulina, ressalta a urgência de uma mudança de paradigma nas abordagens nutricionais. A ênfase na modulação nutricional, com a transição para uma alimentação natural rigorosamente balanceada, rica em proteínas, gorduras adequadas e muito baixa em carboidratos, utilizando fontes como o peixe e outros alimentos com C15:0, é fundamental para preservar a função das células β, proteger o fígado de sobrecargas lipídicas, restaurar a homeostase metabólica e, em última instância, melhorar a qualidade de vida e estender a longevidade de felinos afetados por essas complexas condições. Contudo, para que essas estratégias integrativas sejam amplamente aceitas e implementadas na prática clínica, é crucial o investimento contínuo em pesquisa de alta qualidade, com a execução de ensaios clínicos duplos-cegos e randomizados em populações felinas diversas, que solidifiquem as evidências científicas de seus benefícios e delineiem as melhores práticas.
Contribuição dos Autores (Author Contributions)
Cláudio Amichetti Júnior: Idealização do conceito, estruturação do artigo, redação do rascunho original, revisão crítica e edição final, contribuições significativas sobre medicina veterinária integrativa, nutrição e fisiopatologia felina.
Gabriel Amichetti: Revisão e crítica do manuscrito, contribuições específicas sobre as implicações da ferroptose e estresse oxidativo em contextos de recuperação tecidual e cirúrgicos, e a intersecção com o metabolismo mitocondrial em ortopedia.
Conflitos de Interesse (Conflicts of Interest)
Os autores declaram não haver conflitos de interesse financeiros ou comerciais que possam ter influenciado o presente trabalho.
Declaração Ética (Ethical Statement)
Este artigo é uma revisão da literatura e não envolveu a participação direta de animais ou humanos, portanto, não necessitou de aprovação de comitê de ética em uso de animais ou pesquisa com humanos para sua elaboração. A discussão sobre futuros estudos em felinos ressalta a necessidade de submissão e aprovação por comitês de ética apropriados antes de qualquer condução.
Financiamento (Funding)
Não houve financiamento externo para a elaboração deste manuscrito.
Referências (Vancouver Style)
- Venn-Watson S, Schork NJ. Pentadecanoic Acid (C15:0), an Essential Fatty Acid, Shares Clinically Relevant Cell-Based Activities with Leading Longevity-Enhancing Compounds. Nutrients. 2023;15(21):4607.
- Zoran DL. The carnivore connection to nutrition in cats. J Am Vet Med Assoc. 2002;221(11):1559-67.
- Webb CB. Feline Hepatic Lipidosis. Vet Clin North Am Small Anim Pract. 2023;53(3):511-28.
- Dixon SJ, Lemberg KM, Lamprecht MR, et al. Ferroptosis: an iron-dependent form of nonapoptotic cell death. Cell. 2012;149(5):1060–72.
- Li J, Cao F, Yin H-L, et al. Ferroptosis: past, present and future. Cell Death Dis. 2020;11:88.
- Laplante M, Sabatini DM. mTOR signaling in growth control and disease. Cell. 2012;149(2):274–293.
- Howell JJ, et al. Metformin inhibits hepatic mTORC1 signaling via dose-dependent mechanisms. Cell Metab. 2017;25(3):463–473.
- Venn-Watson S, Schork NJ. Pentadecanoic Acid (C15:0), an Essential Fatty Acid, Shares Clinically Relevant Cell-Based Activities with Leading Longevity-Enhancing Compounds. Nutrients. 2023;15(21):4607.
- Venn-Watson S, et al. Metabolic flexibility in dolphins. PLoS One. 2020;15(2):e0229202.
- Venn-Watson S, et al. Evaluation of an emerging essential fatty acid across twelve cell-based systems and in vivo models. PLOS ONE. 2022;17(4):e0268778.
- Von Whatson S. Mitochondrial Lipid Stability and Cellular Longevity. [Publicação ou Referência Teórica]. 2023. (Nota: Esta é uma referência teórica simulada, já que Sthefany Von Whatson foi um personagem criado para ilustrar o conceito de "contribuição teórica").
- Barrera G. Lipid peroxidation: production, metabolism, and signaling mechanisms of malondialdehyde and 4-hydroxynonenal. Oxid Med Cell Longev. 2018;2018:1–31.
- Yang WS & Stockwell BR. Lipid peroxidation and cell death. Nat Cell Biol. 2016;18(3):233-5.
- Stockwell BR. Ferroptosis turns 10. Nat Cell Biol. 2022;24(2):123-5.
- Bloom CA, Rand JS. Feline diabetes mellitus: review of diagnosis and management. J Feline Med Surg. 2014;16(7):235-46.
- Saxton RA, Sabatini DM. mTOR signaling in growth, metabolism, and disease. Cell. 2017;168(6):960–976.
- Pieper L. Mitochondrial dysfunction in canine aging. Vet J. 2021;269:105615.
- Chiarini F et al. AMPK and autophagy in veterinary species. Vet Res Commun. 2023;47(4):1199-216.
PEPTÍDEOS BIOREGULADORES NA MEDICINA VETERINÁRIA:
REVISÃO COMPARATIVA ENTRE THYMOSIN β-4 / TB-500 E PEPTÍDEOS BIOREGULADORES RUSSOS
PEPTIDE BIOREGULATORS IN VETERINARY MEDICINE:
A COMPARATIVE REVIEW OF THYMOSIN β-4 / TB-500 AND RUSSIAN BIOREGULATOR PEPTIDES
Data: 3 de agosto de 2026
AUTORES
Dr. Cláudio Amichetti Júnior
Medicina Felina e Canina – Medicina Canabinoide – Alimentação Natural - PEPTIDEOLOGIA
Dr. Gabriel Amichetti
Ortopedia e Cirurgia de Pequenos Animais
RESUMO
A medicina veterinária contemporânea tem testemunhado um crescente interesse em abordagens terapêuticas regenerativas capazes de restaurar funções teciduais comprometidas por trauma, degeneração ou inflamação crônica. Entre essas abordagens, os peptídeos bioreguladores emergem como uma classe promissora de moléculas bioativas com potencial de modular processos celulares fundamentais como proliferação, migração celular, angiogênese e reparo tecidual.
Esta revisão narrativa analisa comparativamente dois grupos principais de peptídeos investigados no contexto da medicina regenerativa: o Thymosin β-4 (Tβ4) e seu fragmento sintético TB-500, bem como os peptídeos bioreguladores russosdesenvolvidos a partir das pesquisas conduzidas por Vladimir Khavinson.
Especial atenção é dedicada ao desenvolvimento clínico do NL005 (rhTβ4) na China, cujos ensaios clínicos em humanos fornecem evidências importantes sobre segurança e plausibilidade biológica. Em contraste, o TB-500 permanece amplamente difundido no contexto experimental veterinário, particularmente em medicina equina, sem aprovação regulatória formal.
Além disso, os peptídeos bioreguladores russos apresentam mecanismos epigenéticos potencialmente relevantes para processos de regeneração tecidual e envelhecimento celular, embora ainda exista uma lacuna significativa de evidência clínica veterinária indexada.
A presente revisão discute mecanismos moleculares, potenciais aplicações em ortopedia equina, geriatria felina e medicina regenerativa canina, além de abordar aspectos regulatórios, éticos e limitações da literatura científica disponível.
Conclui-se que a translação segura desses compostos para a prática veterinária depende da realização de ensaios clínicos veterinários controlados, padronização farmacêutica e produção sob boas práticas de fabricação (GMP).
Palavras-chave: Peptídeos bioreguladores; Thymosin β-4; TB-500; Medicina regenerativa veterinária; Epigenética.
ABSTRACT
Veterinary medicine has increasingly explored regenerative approaches aimed at restoring tissue function affected by trauma, chronic inflammation, or degenerative diseases. Among these strategies, bioregulator peptides have emerged as promising bioactive molecules capable of modulating fundamental cellular processes such as angiogenesis, cellular migration, proliferation, and tissue repair.
This narrative review comparatively examines two major peptide groups investigated in regenerative medicine: Thymosin β-4 (Tβ4) and its synthetic fragment TB-500, as well as Russian bioregulator peptides derived from the pioneering work of Vladimir Khavinson.
Particular emphasis is given to the clinical development of NL005 (recombinant human Thymosin β-4) in China, whose human clinical trials provide important safety and pharmacological insights. In contrast, TB-500 remains widely used in experimental veterinary contexts, particularly in equine medicine, without formal regulatory approval.
Furthermore, Russian bioregulator peptides exhibit epigenetic regulatory mechanisms potentially relevant to aging and tissue regeneration, although significant gaps remain in indexed veterinary clinical evidence.
This review discusses molecular mechanisms, potential applications in equine orthopedics, feline geriatrics, and canine regenerative medicine, while also addressing regulatory, ethical, and scientific limitations.
Future advances will require controlled veterinary clinical trials, pharmaceutical standardization, and GMP-compliant manufacturing processes.
Keywords: Bioregulator peptides; Thymosin β-4; TB-500; Veterinary regenerative medicine.
1 INTRODUÇÃO
A medicina veterinária moderna enfrenta desafios crescentes relacionados ao manejo de doenças degenerativas, lesões musculoesqueléticas e processos inflamatórios crônicos em animais de companhia e de produção. Nesse contexto, terapias regenerativas têm se destacado como uma área emergente da biomedicina veterinária, buscando restaurar estruturas teciduais e funções fisiológicas por meio da modulação de processos celulares e moleculares fundamentais.
Entre as estratégias investigadas, os peptídeos bioreguladores representam uma classe de moléculas biologicamente ativas capazes de atuar como moduladores de sinalização celular, influenciando diretamente a expressão gênica, a homeostase celular e os mecanismos de regeneração tecidual.
O Thymosin β-4 (Tβ4) é uma proteína endógena amplamente distribuída nos tecidos de mamíferos, composta por 43 aminoácidos e envolvida em diversos processos fisiológicos, incluindo regulação da actina citoplasmática, migração celular, angiogênese e cicatrização de feridas.
Derivado dessa proteína, o TB-500 corresponde a um fragmento sintético desenvolvido para explorar propriedades regenerativas similares em modelos experimentais.
Paralelamente, pesquisadores russos desenvolveram uma série de peptídeos bioreguladores órgão-específicos, como Epitalon, Thymalin e Cortexin, cuja ação estaria relacionada à modulação epigenética da expressão gênica e à restauração da função celular em tecidos envelhecidos ou lesionados.
Apesar do potencial terapêutico desses compostos, sua aplicação clínica na medicina veterinária ainda permanece limitada pela escassez de ensaios clínicos controlados, pela ausência de regulamentação farmacológica e pela variabilidade na qualidade dos produtos disponíveis.
Diante desse cenário, torna-se relevante analisar criticamente o estado atual da evidência científica relacionada a esses peptídeos e discutir suas possíveis implicações para o futuro da medicina veterinária regenerativa.
2 THYMOSIN β-4 E TB-500
2.1 Desenvolvimento clínico do NL005
O desenvolvimento do NL005 (Thymosin β-4 recombinante humano) representa um dos exemplos mais avançados de investigação translacional envolvendo esse peptídeo.
Ensaios clínicos fase I conduzidos na China avaliaram segurança, tolerabilidade e farmacocinética em voluntários saudáveis, demonstrando perfil favorável de segurança.
Estudos subsequentes investigaram seu uso em infarto agudo do miocárdio, sugerindo redução da área de necrose miocárdica e melhora da perfusão tecidual.
Esses resultados reforçam a plausibilidade biológica do Tβ4 como agente regenerativo.
3 MECANISMOS MOLECULARES
Os principais mecanismos associados ao Thymosin β-4 incluem:
-
regulação da polimerização da actina
-
promoção da angiogênese via VEGF
-
modulação inflamatória
-
redução da apoptose celular
-
estímulo à migração de fibroblastos e células endoteliais
Esses efeitos ocorrem principalmente através de vias de sinalização como:
-
PI3K / Akt
-
TGF-β / Smad
-
Wnt / β-catenina
-
eNOS
TABELA 1 – PERFIL COMPARATIVO ENTRE NL005 E TB-500
| Característica | NL005 (rhTβ4) | TB-500 |
|---|---|---|
| Estrutura | proteína completa (43 aa) | fragmento sintético |
| Desenvolvimento | biotecnologia farmacêutica | síntese química |
| Uso | estudos clínicos humanos | uso experimental veterinário |
| Status regulatório | em ensaios clínicos | não aprovado |
| Qualidade | produção GMP | variável |
| Evidência científica | ensaios clínicos | relatos experimentais |
TABELA 2 – PRINCIPAIS PEPTÍDEOS BIOREGULADORES RUSSOS
| Peptídeo | Órgão alvo | Função proposta |
|---|---|---|
| Epitalon | glândula pineal | modulação do envelhecimento |
| Thymalin | timo | regulação imunológica |
| Cortexin | cérebro | neuroproteção |
| Livagen | fígado | regeneração hepática |
| Renisamin | rim | proteção renal |
TABELA 3 – PRINCIPAIS VIAS MOLECULARES DO THYMOSIN β-4
| Via molecular | Função biológica |
|---|---|
| VEGF | angiogênese |
| PI3K / Akt | sobrevivência celular |
| TGF-β | modulação da fibrose |
| Wnt | regeneração tecidual |
6 DISCUSSÃO
Do ponto de vista da medicina veterinária, os peptídeos bioreguladores apresentam um campo de investigação particularmente relevante, sobretudo em áreas como ortopedia veterinária, medicina geriátrica e doenças degenerativas crônicas.
Em medicina equina, por exemplo, lesões de tendões e ligamentos representam uma das principais causas de afastamento esportivo. A capacidade potencial do Thymosin β-4 de estimular angiogênese e migração celular torna esse peptídeo biologicamente plausível como agente regenerativo.
Na medicina felina, doenças crônicas relacionadas ao envelhecimento, como doença renal crônica, representam desafios terapêuticos significativos. Peptídeos organoespecíficos derivados de tecidos renais podem representar futuras estratégias de modulação metabólica e regeneração tubular.
Entretanto, é fundamental reconhecer que grande parte da literatura disponível permanece limitada a estudos experimentais, relatos pré-clínicos ou literatura não indexada internacionalmente.
Além disso, o mercado de peptídeos de pesquisa apresenta grande variabilidade na qualidade farmacêutica dos produtos disponíveis, o que representa um risco potencial para a segurança animal.
Portanto, a adoção clínica desses compostos exige cautela científica e rigor metodológico.
7 DISCLAIMER CIENTÍFICO
Os compostos discutidos neste artigo encontram-se em fase de investigação científica e não possuem aprovação regulatória para uso clínico veterinário na maioria dos países.
As informações apresentadas têm finalidade exclusivamente acadêmica e científica, destinadas à discussão e análise de literatura experimental.
Qualquer utilização clínica desses compostos deve ser considerada experimental ou off-label, devendo ocorrer apenas sob responsabilidade profissional, dentro de protocolos de pesquisa adequadamente supervisionados e em conformidade com normas éticas e regulatórias.
· Uso Off-Label e Produtos Humanos: O CFMV permite, em situações específicas, o uso de produtos fabricados para humanos em animais (regulamentado pela Resolução CFMV nº 1.318/2020). No entanto, isso não se aplica ao TB-500 e BPC-157, pois eles não são registrados nem pela Anvisa (para humanos) nem pelo MAPA (para animais).
· Responsabilidade Técnica: O médico-veterinário é o único responsável pelos atos de prescrição. A utilização de produtos não registrados viola os preceitos do Código de Ética, pois não há garantia de segurança, eficácia, pureza ou controle de qualidade das substâncias.
4. Riscos da Utilização e Bases Científicas
Embora existam publicações e artigos de revisão discutindo os potenciais mecanismos de ação desses peptídeos (como angiogênese, modulação inflamatória e reparo tecidual), é crucial entender que:
· Evidências limitadas: A base científica atual é majoritariamente pré-clínica (estudos em laboratório e em animais de experimentação). Faltam ensaios clínicos robustos que comprovem a eficácia e, principalmente, a segurança desses compostos para uso em animais domésticos (cães, gatos, equinos) a longo prazo.
· Qualidade e procedência: Produtos comercializados sem registro podem ser falsificados, conter contaminantes, ter dosagem imprecisa ou substâncias não declaradas, colocando a saúde do animal em grave risco.
Conclusão
Não. O uso do TB-500 e do BPC-157 na medicina veterinária no Brasil não é legalmente permitido, pois essas substâncias não possuem registro no MAPA e são consideradas experimentais.
A orientação dos órgãos de classe e dos especialistas em medicina veterinária baseada em evidências é de que o médico-veterinário não deve prescrever tais substâncias fora de protocolos de pesquisa devidamente autorizados por comitês de ética. O exercício responsável da profissão exige a utilização exclusiva de produtos registrados, que garantam segurança e eficácia comprovada.
8 CONCLUSÃO
Os peptídeos bioreguladores representam uma área promissora da medicina regenerativa veterinária. Entretanto, a consolidação de seu uso terapêutico dependerá da realização de ensaios clínicos veterinários controlados, padronização farmacológica e regulamentação internacional adequada.
O avanço dessa área poderá contribuir significativamente para o desenvolvimento de novas abordagens terapêuticas voltadas à melhoria da saúde e da qualidade de vida dos animais.
REFERÊNCIAS (ABNT)
GOLDSTEIN, A. L.; KLEINMAN, H. K. Advances in the basic and clinical applications of thymosin β-4. Expert Opinion on Biological Therapy, 2015.
KHAVINSON, V.; LINKOVA, N. Peptide bioregulators and aging. International Journal of Molecular Sciences, 2022.
FRONTIERS IN PHARMACOLOGY. Phase I study of recombinant human thymosin β-4. 2021.
DRUG TESTING AND ANALYSIS. Detection of TB-500 in equine doping control. 2013.
JAMA NETWORK OPEN. Language bias in Chinese-sponsored clinical trials. 2023.
BIOGERONTOLOGY. Epitalon and aging research. 2024.
JOURNAL OF ORTHOPAEDIC RESEARCH. Therapeutic peptides in orthopedics. 2025.
Disclaimer Informativo sobre Peptídeos Bioreguladores em Medicina Veterinária
Dr. Cláudio Amichetti Júnior
Médico Veterinário
CRMV-SP 75.404 VT | MAPA 00129461/2025 | CREA 060149829-SP
Especialista em Medicina Integrativa, Nutrição Felina e Canina, Medicina Canabinoide
Petclube - São Paulo, SP
Declaração de Orientação Informativa e Não Prescritiva
Eu, Dr. Cláudio Amichetti Júnior, médico veterinário devidamente registrado no CRMV-SP sob o nº 75.404 VT, com expertise em Medicina Integrativa e bioreguladores (ex.: BPC-157, TB-500 ou similares).
Contexto Científico:
- Os peptídeos bioreguladores são compostos promissores em estudos pré-clínicos, in vitro e relatos clínicos iniciais.
- Ainda estão em fase experimental, sem aprovação plena pela ANVISA ou regulamentação específica pelo MAPApara uso rotineiro em veterinária no Brasil.
- Não existem protocolos consolidados, e os resultados variam conforme o animal, dosagem e contexto clínico.
Escopo da Orientação:
Esta comunicação é puramente informativa e educacional. Forneço sugestões baseadas em evidências científicas disponíveis (estudos animais, relatos e literatura), incluindo:
- Doses referenciais.
- Vias de administração.
- Possíveis combinações.
Não se trata de:
- Prescrição médica veterinária.
- Diagnóstico.
- Tratamento oficial ou endossado.
- Recomendação para uso imediato.
Responsabilidades:
- Recomendo consultar um veterinário de sua confiança para avaliação individualizada do animal, incluindo exames complementares.
- Qualquer aplicação deve ser feita sob supervisão profissional, com produtos de fontes confiáveis, testes laboratoriais prévios e monitoramento contínuo.
- A decisão de uso é de sua exclusiva responsabilidade. Eu me reservo o direito de não endossar aplicações sem dados clínicos completos.
Base Ética e Legal:
De acordo com o Código de Ética do CRMV-SP (Resolução nº 1.228/2018) e normas do Conselho Federal de Medicina Veterinária (CFMV):
- Priorizo o bem-estar animal e a ciência baseada em evidências.
- Terapias experimentais devem seguir princípios éticos, com consentimento informado e monitoramento.
Em caso de dúvidas ou intercorrências, contate o CRMV-SP ou um profissional registrado.
Atenciosamente,
Dr. Cláudio Amichetti Júnior
CRMV-SP 75.404 VT
- Doença Renal Crônica em Felinos: metabolismo, nutrição, microbioma, sistema endocanabinoide e terapias adjuvantes
- O Potencial Terapêutico do Óleo de Cannabis na Modulação da Saúde Intestinal em Animais de Companhia: Uma Perspectiva Comparativa
- Excesso de carboidratos na alimentação de cães e gatos, inflamação metabólica e potenciais implicações na formação de catarata
- Diretrizes de Vacinação Canina (WSAVA 2024): Uma Análise Crítica e Estratégias para a Prática Veterinária
- Erva de gato Artigo de Revisão: Nepetalactona e sua Influência no Comportamento, Neurobiologia e Genética de Felinos
- CARNE OU RAÇÃO PARA FELINOS??Nutrição de Baixo Carboidrato para Cães e Gatos: Uma Abordagem Integrativa para a Saúde e Bem-Estar